Папилломавирусная инфекция и беременность. Особенности диагностики и тактики ведения
В статье представлены особенности взаимодействия вируса папилломы человека (ВПЧ) с иммунной системой, сделан акцент на особую актуальность ВПЧ-инфекции во время беременности и риск развития папилломавирусной патологии у детей. Приведены данные собственног
The article presents the features of interaction of human papilloma virus (HPV) with the immune system, emphasizes the special relevance of HPV infection during pregnancy and the risk of papillomavirus pathology in children. The data of own research of frequency of occurrence of HPV-associated pathology of extragenital localization in pregnant women with the diagnosis of anogenital warts were presented.
Распространенность папилломавирусной инфекции (ПВИ) и соответственно связанная с ней патология на протяжении последних десятилетий во многих странах мира, включая Россию, неуклонно увеличиваются. По данным литературы ежегодно в мире регистрируется до 3 млн новых случаев заражения вирусом папилломы человека (ВПЧ) [1]. Передача ВПЧ от человека к человеку может осуществляться несколькими путями: контактно-бытовым, вертикальным, при генитальных, оральных, аногенитальных контактах. Высокий рост инфицированности населения ВПЧ, обусловленный его значительной контагиозностью, многообразие вариантов патологии, ассоциированной с ним, и, главное, способность трансформировать эпителиальные клетки, запуская процесс канцерогенеза, привлекают внимание различных специалистов к поиску вариантов лечения, своевременной диагностике и профилактике заболеваний, ассоциируемых с ВПЧ [2, 3]. При этом особое внимание уделяется ПВИ урогенитального тракта, которая занимает лидирующие позиции по распространенности среди инфекций, передающихся половым путем. Активность развития и формирование ВПЧ-ассоциированной, как и другой инфекционной патологии во многом определяются состоянием иммунной системы и ее способностью адекватно реагировать на наличие патогена. Вместе с тем ВПЧ, блокируя определенные звенья иммунитета и проявляя устойчивость к ФНО-опосредованному ингибированию пролиферации, что связано со значительным снижением экспрессии ФНО-рецепторов, способен «уходить» из-под системы иммунологического надзора [4–6]. Установлено, что ВПЧ за счет активации убиквитинопосредованного протеолиза белка р53, являющегося супрессором канцерогенеза, способен влиять на механизмы регуляции молекулярно-генетического цикла деления клеток и блокировать апоптоз [7–9]. Доказано также, что белок Е7 ВПЧ нейтрализует противовирусную и противоопухолевую активность интерферона-α2 за счет его способности избирательно блокировать большинство генов, индуцируемых интерфероном [10]. Такие разнонаправленные механизмы взаимодействия ВПЧ с иммунной системой организма человека способствуют выживаемости, длительной персистенции вируса и высокому риску развития ВПЧ-ассоциированной патологии, особенно при наличии триггерных факторов.
Последовательная и целостная картина эпидемиологии и патогенеза ПВИ, сложившаяся в течение последних двух десятилетий, более четко представляется в отношении женщин, нежели мужчин [11]. ПВИ у них регистрируют в 40%, 70% и более 90% случаев рака вульвы, влагалища и шейки матки соответственно, являющихся второй по значимости причиной смерти женщин во всем мире [11–14]. В последнее время с раком цервикального канала шейки матки (95%) связывают около 20 типов ВПЧ, среди них наиболее часто выявляются ВПЧ 16-го типа (50%) и ВПЧ 18-го типа (10%) [15]. Необходимо отметить, что помимо ВПЧ в развитии онкогенной трансформации определяющую роль играет целый ряд сопутствующих факторов. Здесь прежде всего следует выделить сопутствующие инфекционные заболевания аногенитальной области. Неблагоприятна, особенно в плане развития цервикальных дисплазий, сочетанная персистенция ВПЧ с ВПГ 2-го типа, ЦМВ, ВЭБ, ВИЧ, хламидиями и микоплазмами. Особое значение, как уже было сказано выше, в возникновении инфекции, тяжести ее течения, исходе, качестве и контроле процесса терапии больных с патологией кожи и урогенитального тракта, обусловленными ВПЧ, имеет характер иммунного ответа [16].
Одной из особенностей ВПЧ-инфекции урогенитального тракта считается ее широкое распространение среди молодых женщин репродуктивного возраста, преимущественно до 25 лет [17], что обусловлено низкой сексуальной культурой населения, частой сменой половых партнеров, незащищенным сексом, вредными привычками (курение, токсикомания, алкоголизм). Отмечается рост заболеваемости детей препубертатного возраста и подростков аногенитальными бородавками, что частично можно объяснить увеличением числа детей, рано начинающих половую жизнь. По данным социологических опросов наличие половых контактов в своей жизни отметили около 15% девочек и 22% мальчиков, при этом 50% из них указали, что первый половой контакт был совершен в возрасте до 15 лет, а у 5% девочек и 20% мальчиков — до 12 лет [16]. Вместе с тем отмечено, что у подростков и молодых женщин чаще и быстрее происходит самопроизвольная элиминация ВПЧ (до 80% случаев) и регрессия имеющейся ВПЧ-ассоциированной патологии по сравнению с женщинами более позднего возраста. По результатам исследований, среднее время элиминации ВПЧ у подростков составляет 8 месяцев (CDC, 1999). По наблюдениям С. И. Роговской и В. Н. Прилепской (2006) у каждой второй пациентки в возрасте 18–25 лет этот период увеличивается до 1,5–2 лет.
Особую актуальность ВПЧ-инфекция приобретает во время беременности, при этом частота регистрации всех типов ВПЧ у беременных женщин составляет 30–65%, а типов высокого онкогенного риска — 20–30% [18].
Основная особенность беременности заключается в том, что плод по отношению к матери является генетически наполовину чужеродным (полуаллогенным) организмом, который до положенного срока не отторгается. Аллогенность плода заключается в том, что все клетки содержат помимо гаплоидного набора HLA-антигенов матери, гаплоидный набор HLA-антигенов отца. Созревание оплодотворенной яйцеклетки до зрелого плода в наполовину чужеродном организме матери осуществляется за счет супрессорного механизма, который развивается с первых часов после зачатия и действует до развития родовой деятельности. Этот механизм не позволяет иммунной системе матери осуществлять иммунную атаку на плод с целью отторжения на всех этапах его развития [19].
Развивающаяся после зачатия супрессия многофакторна и формируется как за счет продуктов эндокринной системы, так и за счет определенных изменений системных и местных иммунных реакций, выработавшихся в процессе эволюции для защиты полуаллогенного плода от иммунной системы матери: отсутствие на клетках трофобласта классических антигенов системы HLA класса I и II; сдвиг функционального баланса Т-хелперов в сторону клеток 2-го типа и иммунорегуляторная роль плаценты, обеспечивающая своеобразный иммуносупрессивный фон в организме матери [20].
Таким образом, само оплодотворение имеет под собой иммунную природу. Активные процессы, направленные на локальную иммуносупрессию, осуществляются в течение всей беременности в фетоплацентарном комплексе.
В такой ситуации ПВИ является не только высоким риском развития ВПЧ-ассоциированной патологии на фоне физиологического иммунодефицита, но и возможности передачи ее от матери к ребенку во время родов [21]. В 1989 г. доказана вертикальная передача вируса, что подтверждают сообщения об обнаружении ВПЧ в амниотической жидкости беременных и у детей, рожденных от матерей — носителей ВПЧ [22]. Возможный риск колеблется по данным разных авторов от 3% до 80% [23]. Данный разброс объясняется различиями в методике проведения полимеразной цепной реакции (ПЦР) на выявление ДНК ВПЧ. При этом ПВИ может передаваться трансплацентарно и интранатально (в частности, ВПЧ 6-го и 11-го типа). Риск инфицирования прямо пропорционален тяжести инфекции (количеству вирусных частиц) и времени безводного промежутка в родах, однако проведенные исследования свидетельствуют о том, что родоразрешение путем кесарева сечения не снижает риск инфицирования плода, что свидетельствует о преимущественно внутриутробном его заражении [22]. Интранатальное инфицирование может приводить к ювенильному рецидивирующему респираторному папилломатозу (частота составляет 1,7–2,6 на 100 000 детей и 1 на 1500 родов среди женщин с генитальной ПВИ) [24].
Инвазия вируса происходит через микроповреждения кожи и слизистых с инфицированием преимущественно незрелых, делящихся клеток базального слоя эпителия, которые являются для ВПЧ клетками-мишенями. Далее происходит репликация вируса и сборка вирусных частиц в дифференцированных клетках поверхностного слоя эпителия. При этом ВПЧ могут оказывать на эпителий продуктивное или трансформирующее воздействие. При продуктивном воздействии возникают доброкачественные новообразования — папилломы, бородавки и кондиломы кожи и слизистых оболочек. Результатом трансформирующего воздействия являются дисплазии различной степени тяжести, прогрессирующее развитие которых приводит к раку [25, 26]. Веские доказательства об ускорении развития аногенитального рака и увеличение онкологического риска при ранней экспозиции ПВИ подчеркивают особую важность не только изучения распространенности ПВИ у детей, а, главное, регулярное и длительное наблюдение за ними, учитывая возможность развития в том числе и аногенитальной неоплазии [27].
В литературе имеются исследования, доказывающие, что при подтвержденной ПЦР ПВИ у матери структурное повреждение компонентов последа в конце беременности определяется в 76,8% случаев и протекает с морфофункциональными признаками хронической плацентарной недостаточности, гипотрофии плода и осложнениями неонатального периода [28, 29].
В настоящее время отмечается увеличение и рост папилломатоза гортани как у взрослых, так и у детей. При этом у взрослых превалирует передача инфекции при ороаногенитальных контактах, а у детей при прохождении через инфицированные родовые пути и контактно-бытовым путем.
Манифестация ювенильного респираторного папилломатоза в 75–85% случаев регистрируется в первые 5 лет жизни; в 5–6% случаев у детей от 6 месяцев до года; в 45% случаев у детей до 3 лет [28].
Клиническая картина респираторного папилломатоза складывается из нарушения голоса и дыхания. Наиболее часто при поражении гортани в области комиссуры и передних отделов голосовых складок развивается охриплость голоса, вплоть до полной его потери. По мере сужения просвета гортани папилломами развивается стеноз, возможна смерть от асфиксии. Патологический процесс в детском возрасте носит активный характер, для него характерны распространенность и частота рецидивирования, в связи с чем дети подвергаются многократным хирургическим вмешательствам с целью удаления папиллом. Многократная повторная эксцизия ларингеальных опухолей приводит к развитию рубцовых осложнений, необходимости трахеостомии, к потере способности говорить, усугублению хронической респираторной гипоксемии. При прогрессировании и распространении опухоли в дистальные дыхательные пути заболевание часто заканчивается фатальным исходом [24].
Учитывая, что заражение ПВИ ребенка с развитием ювенильного рецидивирующего респираторного папилломатоза возможно не только в интранатальном, а и постнатальном периоде, а также нередкую регистрацию ВПЧ-ассоциированной патологии у новорожденных и детей раннего детского возраста, следует более активно и тщательно обследовать пациентов на этапе как планирования беременности, так и во время беременности. При этом внимание уделять не только обследованию на высокоонкогенные типы ВПЧ, но и низкоонкогенные, учитывая, что, как правило, у пациентов, страдающих рецидивирующим респираторным папилломатозом, чаще обнаруживают низкоонкогенные ВПЧ 6-го и/или 11-го типа, они же нередко регистрируются и при аногенитальных бородавках и остороконечных кондиломах на других участках кожи и слизистой.
Целью исследования было оценить частоту ВПЧ-ассоциированной патологии кожи и слизистых не генитальной локализации у беременных с установленным диагнозом «аногенитальные бородавки».
Материал и методы исследования
Под наблюдением находились 76 беременных женщин (срок беременности от 12 до 26 недель) в возрасте от 18 до 42 лет с установленным клиническим диагнозом аногенитальных (венерических) бородавок. Средний возраст пациенток составил 26,3 года. У 53 (69,7%) пациентов длительность заболевания составила от 3 нед до 6 мес, у 23 (30,3%) пациентов — от 6 мес до 1 года. 18 (23,7%) пациенток констатировали о рецидивах аногенитальных бородавок после ранее проведенного лечения методами деструкции (лазерной вапоризации, электрохирургическим иссечением, криодеструкцией). Все пациентки были направлены из женских консультаций на удаление аногенитальных бородавок. Из них только у 2 (2,6%) пациенток отмечено сочетание остороконечных кондилом аногенитальной и экстрагенитальной локализации. У 42 (55,3%) больных, включенных в исследование, ПВИ подтверждалась идентификацией ВПЧ методом полимеразной цепной реакции в режиме реального времени (ПЦР-RT): ДНК ВПЧ типов 16, 31, 33, 35, 52, 58 были выявлены у 18 (42,9%) пациентов, ВПЧ типов 18, 39, 45, 59 — у 14 (33,3%), ВПЧ типов 51, 56 — у 10 (23,8%); на ВПЧ низкого онкогенного типа из них были обследованы только 6 (14,3%) пациенток: 6-й и 11-й типы обнаружены у 5 из них (11,9%). Идентификация ВПЧ методом ПЦР-RT или другим лабораторным методом не проводилась у 34 (44,7%) пациенток. Результаты исследования: при физикальном осмотре пациенток на момент их обращения за медицинской помощью у 39 (51,3%) пациенток были обнаружены остроконечные кондиломы на коже и слизистых экстрагенитальных областей: у 14 (35,9%) на коже соска и околососковой области; у 11 (28,2%) на коже конечностей; у 9 (23,1%) — на коже пупка; у 5 (12,8%) — на слизистой полости рта. В аногенитальной области папилломатозные разрастания регистрировались на коже больших половых губ — у 5 (6,6%), слизистой оболочке вульвы — у 30 (39,5%), в области задней спайки — у 4 (5,3%), на слизистой оболочке наружного отверстия уретры — у 2 (2,6%), на коже перианальной и паховых областей — у 4 (5,3%), на слизистой оболочке влагалища — у 48 (63,2%) больных. Сочетанное поражение нескольких анатомических зон аногенитальной области наблюдалось у 15 (19,7%) пациенток.
Всем пациенткам проведено удаление остроконечных кондилом радиоволновым методом. По нашим наблюдениям оптимальным сроком беременности для проведения данной процедуры определен срок гестации после 16 недель, когда заканчивается основной этап формирования плаценты и иммуносупрессивный фон в организме матери значительно снижается, что резко снижает риск возможных рецидивов.
Таким образом, нередкое обнаружение сочетанной ВПЧ-ассоциированной патологии аногенитальных и экстрагенитальных областей у беременных свидетельствует о необходимости более тщательного обследования таких пациенток с целью не только минимизации риска развития осложнений и рецидивирования ВПЧ-ассоциированной патологии, но и исключения инфицирования ребенка. Более глубокое обследование беременных на ВПЧ, включающего не только высокоонкогенные, но и низкоонкогенные типы, даст возможность избежать или значительно снизить риск развития ВПЧ-ассоциированной патологии у детей.
Литература
- Nyitray A. G., Iannacone M. R. The epidemiology of human papillomaviruses // Curr Probl Dermatol. 2014; 45 (1): 75–91.
- Семенов Д. М., Данько С. Н., Дмитраченко Т. И. Папилломавирусная инфекция (клинико-патогенетические особенности, лечение, профилактика). Учебно-методическое пособие. Витибск: Гос. мед. ун-т. СПб: Диалект. 2008. 84 с.
- Киселев В. И. Вирусы папилломы человека в развитии рака шейки матки. М.: Компания «Димитрейд График Групп», 2004. 180 с.
- Рахматуллина М. Р., Нечаева И. А., Шалва Марди. Опыт деструктивной терапии аногенитальных бородавок // Вестник дерматологии и венерологии. 2016. № 5. С. 96–101.
- Tavares M. C., de Lima Junior S. F., Coelho A. V. et al. // Ann Hum Biol. 2015, Jun; 16; 1–8.
- Prabhavathy D., Subramanian C. K., Karunagaran D. Re-expression of HPV16 E2 in SiHa (human cervical cancer) cell potentiates NF-kB activation induced by TNF-α concurrently increasing senescence and survival // Biosci Rep. 2015, Feb; 25; 35 (1).
- Aguilar-Martinez E., Morrisroe C., Sharrocks A. D. The ubiquitin ligase UBE3 A dampens ERK pathway signalling in HPV E6 transformed HeLa cells // PLoS One. 2015. Mar; 27; 10 (3).
- Holloway A., Simmonds M., Azad A., Fox J. L., Storey A. Resistance to UV-induced apoptosis by β-HPV5 E6 involves targeting of activated BAK for proteolysis by recruitment of the HERC1 ubiquitin ligase // Int J Cancer. 2015, Jun; 15; 136 (12): 2831–2843.
- Jing K., Shin S., Jeong S., Kim S., Song K. S., Park J. H., Heo J. Y., Seo K. S., Park S. K., Kweon G. R., Wu T., Park J. I., Lim K. Docosahexaenoic acid induces the degradation of HPV E6/E7 oncoproteins by activating the ubiquitin-proteasome system // Cell Death Dis. 2014, Nov; 13; 5: 1524.
- Сухих Г. Т., Прилепская В. Н., Роговская С. И. и др. Применение препаратов интерферона при лечении плоскоклеточных интраэпителиальных поражений шейки матки низкой степени // Эффективная фармакотерапия в акушерстве и гинекологии. 2009. № 4. С. 36–41.
- Батыршина С. В., Шулаев А. В., Акберова Д. Р. Папилломавирусная инфекция: оптимизация диагностики и лечения // Клиническая дерматология и венерология. 2015. 14 (5). С. 67–77.
- Baldwin A., Pirisi L., Creek K. E. NFI-Ski interactions mediate transforming growth factor beta modulation of human papillomavirus type 16 early gene expression // J Virol. 2004, Apr 1; 78 (8): 3953–3964.
- Byg L. M., Vidlund J., Vasiljevic N. et al. NF-kB signaling is attenuated by the E7 protein from cutaneous human papillomaviruses // Virus Res. 2012, Oct 1; 169 (1): 48–53.
- Grulich A. E., Jin F., Conway E. L. et al. Cancers attributable to human papillomavirus infection // Sex Heath. 2010; 7 (3): 244–252.
- Данилова О. В., Юнусова Е. И. Тактика ведения папилломавирусных поражений гениталий. Учебное пособие для врачей. Казань, 2012. 30 с.
- Юнусова Е. И., Данилова О. В., Гизатуллина Р. Д. ВПЧ-ассоциированная патология урогенитального тракта. Сборник материалов V Всероссийской научно-практической конференции с международным участием «Казанские дерматологические чтения: синтез науки и практики. Казань, 2017. С. 117–121.
- Ван Крог Д., Лейси С. Д., Гросс Д., Баракко Р., Шнайдер А. Европейское руководство по аногенитальным бородавкам // ИППП. 2002. № 3. С. 29–37.
- Szepietowska M., Sfodzifski H. et al. Evaluation of frecuency HPV infection during pregnancy // Ginecol Pol. 2002; 73 (8): 662–665.
- Долгушина Н. В. Иммунологические аспекты развития плацентарной недостаточности и невынашивания беременности у пациенток с хроническими вирусными инфекциями // Акушерство и гинекология. 2008. № 4. С. 16–19.
- Wicherek L., Basta P., Sikora J. at al. RCAS1 decidual immunoreactivity in servere pre-eclampsia: Immune cell pre-cence and activity // Amer. J. Period. Immunol. 2007. V. 68, № 4. P. 358–366.
- Woodhall U. K., Jeet M., Soldan K. et al. Effect of genital warts: the loss of guality of life and cost of treatment in eight sex clinics in the UK // Sex and the transmissions. 2011; 87: 458–463.
- Sedlacek T. V., Lindheim S. et al. Mechanism for HPV transmission at birth // Am J Obstet Gynecol. 1989; 161: 55–59.
- Watts D. H., Koutsky L. A. et al. Low — risk perinatal transmission of HPV: results from a prospective cohort study // Am J Obstet Gynecol. 1989; 178: 365–373.
- Green G. E., Bauman N. M., Smith R. J. Pathogenesis and treatment of juvenile onset recurrent respiratory papillomatosis // Otolaryngol Clin North Am. 2000; 33 (1): 187–207.
- Роговская С. И. Папилломавирусная инфекция у женщин и патология шейки матки. М.: ГЕОТАР-Медиа, 2005. С. 15–17.
- Юнусова Е. И., Юсупова Л. А., Мавлютова Г. И., Гараева З. Ш. Плоские бородавки: особенности и возможности терапии // Лечащий Врач. 2016. № 5. С. 52–55.
- Коколина В. Ф., Малиновская В. В. Папилломавирусная инфекция. Пособие для врачей. М., 2008. 44 с.
- Воробцова И. Н., Тапильская Н. И., Гайдуков С. Н. Результаты обследования новорожденных, рожденных от матерей с различными формами папилломавирусной инфекции // Педиатр. 2011. Т. II. № 4. С. 72–75.
- Чистяков М. А. Патоморфология папилломавирусной инфекции в системе «мать-плацента-плод». Автореф. дис. … к.м.н. М., 2008. 25 с.
Е. И. Юнусова 1 , кандидат медицинских наук
О. В. Данилова, кандидат медицинских наук
Л. А. Юсупова, доктор медицинских наук, профессор
Г. И. Мавлютова, кандидат медицинских наук
З. Ш. Гараева, кандидат медицинских наук
ГБОУ ДПО КГМА МЗ РФ, Казань
Папилломавирусная инфекция и беременность. Особенности диагностики и тактики ведения/ Е. И. Юнусова, О. В. Данилова, Л. А. Юсупова, Г. И. Мавлютова, З. Ш. Гараева
Для цитирования: Лечащий врач № 5/2018; Номера страниц в выпуске: 56-59
Теги: папилломавирусная инфекция, поражение кожи, половой путь распространения
ВПЧ и беременность
Папилломавирусная инфекция сегодня является наиболее распространенным заболеванием с преимущественной передачей половым путем.
Возбудитель инфекции – вирус папилломы человека, сокращенно ВПЧ.
Наибольший риск заражения ВПЧ имеют молодые женщины возраста 20-35 лет.
Хотя в большинстве случаев инфекция протекает бессимптомно и склонна к самоизлечению, иногда папилломавирусы становятся причиной серьезных состояний.
Таких как аногенитальные бородавки и рак шейки матки (93% всех эпизодов последнего заболевания связаны именно с ВПЧ, из которых 70% провоцируются ВПЧ 16-го и 18-го типа).
Особый интерес у женщин репродуктивного возраста вызывает ответ на вопрос о том, влияет ли ВПЧ на беременность?
Дело в том, что во время беременности происходящие изменения в гормональном фоне и иммунной системе организма способствуют «удержанию» ВПЧ, увеличивают риск заражения женщины инфекцией и передачи вируса партнеру.
Кроме того, любая инфекция в организме матери может оказать воздействие на здоровье будущего ребенка.

Что собой представляет инфекция ВПЧ?
Специфической особенностью ВПЧ является его склонность к поражению клеток эпителия кожи и слизистых.
Несколько десятков известных типов вирусов папилломы человека объединяются в три группы по их способности провоцировать онкологические заболевания.
При этом различают:
- неонкогенные, примером которых являются типы 1,2,28, 41 и др., ответственные за появление кожных бородавок (подошвенных, вульгарных и пр.);
- с низким риском развития онкопатологии, такие как типы 6,11, 15, 25, 43 и пр., заражение которыми может проявляться в виде аногенитальных бородавок (иначе остроконечных кондилом) и сопровождаться развитием злокачественных преобразований только в исключительно редких случаях;
- с высоким риском, в том числе типы 16, 18, 33, 52 и др., с инфицированием которыми связывают предраковые/раковые изменения шейки матки, а также такое заболевание, как бовеноидный папуллез.
Как происходит заражение ВПЧ?
Папилломавирусы способны передаваться только от человека к человеку.
Так как некоторые типы могут в течение определенного времени сохраняться в отшелушивающихся клетках кожи, то они могут обуславливать риск контактно-бытового заражения.
Такой вариант характерен для неонкогенной группы, например, вероятно заражение с образованием подошвенных бородавок при наличии микроповреждений кожи стоп.
Низко- и высокоонкогенные вирусы передаются половым путем, включая различные варианты сексуальных контактов.
Изредка встречается заражение новорожденных детей больными матерями.
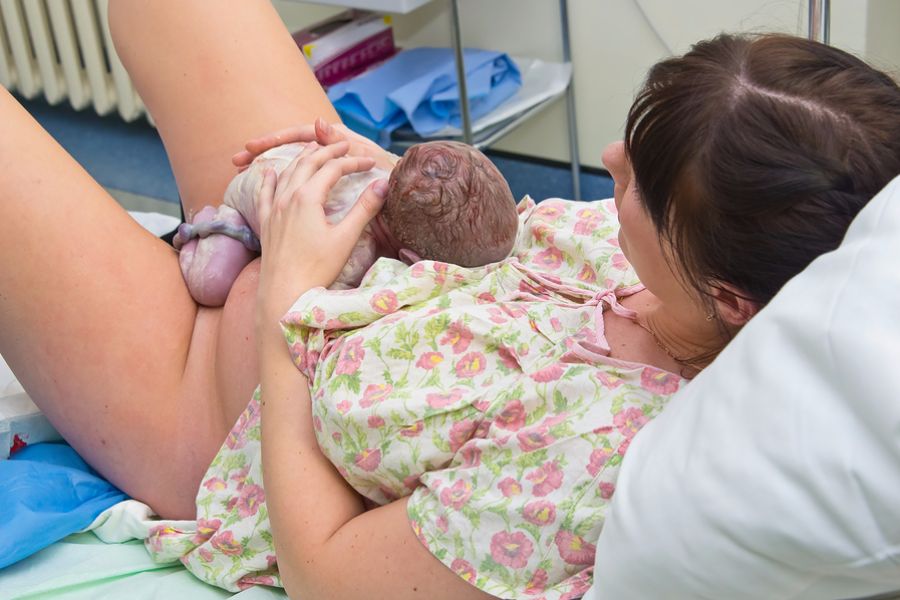
Интересно, что женщины с диабетом, при хорошо контролируемом уровне глюкозы, не имеют повышенного риска инфицирования ВПЧ.
Инкубационный период довольно продолжителен и может варьироваться от трех месяцев до нескольких лет.
Как проявляется инфекция?
Симптомы инфекции определяются типом вируса и видом вызванного им заболевания.
ВПЧ может находиться как вне клеточных хромосом, т. н. доброкачественная форма болезни, так и встраиваться в ДНК, злокачественная форма.
Для папилломавирусной инфекции характерны следующие варианты развития:
- латентное течение – без изменения клеток, без симптомов;
- образование бородавок, кондилом, папиллом, когда вирус воздействует на клетки, провоцируя их разрастание;
- неопластические изменения (дисплазия) – изменение клеточной структуры под влиянием вируса;
- образование карциномы – появление многочисленных атипичных клеток, характерных для раковой опухоли.
Важной особенностью ВПЧ-инфекции является ее способность к самоизлечению.
В 90% всех эпизодов заражения в течение двух лет вирус уничтожается организмом.
Клинические проявления инфекции довольно характерны.
Так, вульгарные бородавки имеют вид серовато-бурых бородавчатых узелков, которые обычно размещаются на пальцах рук и тыльной стороне кистей.
Плоские бородавки поражают лицо и кисти, обычно проявляются в подростковом возрасте.
Подошвенные бородавки появляются в области трения кожи обувью, представляют собой характерные утолщения, болезненные при надавливании.
Остроконечные кондиломы напоминают по форме гребень петуха или кочешок цветной капусты, имеют тонкую ножку и более широкую головку.

У женщин такие образования обычно размещаются у входа во влагалище, в области половых губ и заднего прохода. Множественные плоские папулы, как проявление инфекции, вызванной ВПЧ низкого онкогенного риска, называются бородавчатой эпидермодисплазией.
При ларингеальном папилломатозе типичные выросты выявляются в области гортани.
Куполообразные и плоские гладкие, бархатистые папулы на гениталиях служат характерным проявлением бовеноидного папулеза.
Причиной которого является преимущественно ВПЧ-16 (представитель группы высокого онкогенного риска).
Озлокачествление подобных образований наблюдается примерно в 3% эпизодов.
Дисплазия (неоплазия) шейки матки – это процесс атипичного изменения эпителиальных клеток в зоне перехода плоского эпителия в цилиндрический.
Такое состояние относится к предраковым.
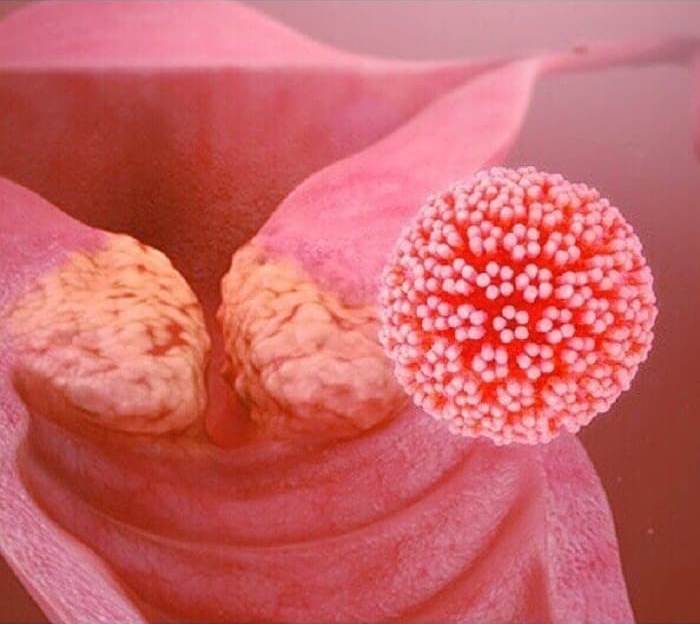
В зависимости от выраженности изменения клеток выделяют разные степени дисплазии и собственно рак (плоскоклеточную карциному).
Способствуют развитию дисплазий:
- многократные беременности и роды в возрасте до 20-ти лет;
- раннее начало половой жизни;
- беспорядочные половые связи;
- хроническое воспаление маточной шейки;
- поражение остроконечными кондиломами;
- курение и пр.
Каковы последствия ВПЧ при беременности?
На сегодняшний день нет достоверных доказательств выраженного негативного воздействия инфекции на течение беременности.
Такие характерные для иных половых инфекций патологии беременности, как невынашивание, преждевременные роды и т. п., не нашли безусловного подтверждения связи с ВПЧ.
Тем не менее, если первичное инфицирование женщины произошло именно в период беременности, риск развития различных осложнений присутствует.
Некоторые последствия для плода при беременности имеют аногенитальные бородавки у матери, вызванные ВПЧ 6 и 11 типа, с локализацией в области малых половых губ и преддверия влагалища.
Такие остроконечные кондиломы несут небольшой риск заражения плода в родах, приводя к развитию у последнего респираторного папилломатоза.
Респираторный, или иначе ларингеальный, папилломатоз (также называемый папилломатозом гортани) чаще всего развивается у детей 2-х – 3-х лет.

В результате заражения от больной матери еще в период беременности последней или непосредственно при рождении.
Путь передачи во время беременности через плаценту, в ходе родов или непосредственно после них, пока не вполне ясен.
Основными симптомами заболевания являются осиплость, вплоть до полного исчезновения голоса, и затруднения глотания.
По мере прогрессирования болезни появляются отдышка, кашель.
В тяжелых ситуациях возможно перекрывание верхних дыхательных путей, асфиксия, особенно в случае образований с длинной тонкой ножкой.
В процессе осмотра посредством ларингоскопа (иногда применяется и бронхоскоп) на слизистой гортани обнаруживаются типичные разрастания – кондиломы.
Такая патология отличается довольно агрессивным течением: после удаления образований часто происходят рецидивы, требующие повторных хирургических вмешательств.
Если наступает беременность при инфицировании папилломавирусами высокой онкогенности (особенно ВПЧ 16, 18), женщина должна обязательно сообщить о наличии инфекции своему акушеру-гинекологу.
Дело в том, что изменения в организме беременной женщины могут спровоцировать более интенсивное преобразование клеток.
Собственно, на течение самой беременности, на ребенка такие вирусы не оказывают влияния, но создают определенную угрозу здоровью женщины.
В ситуации, когда инфекции в прошлом выявлено не было, при постановке на учет среди прочих берется и цитологический мазок по Папаниколау (ПАП-тест).

Если анализ показывает отклонения, то врач назначает дополнительные исследования (например, кольпоскопию).
Также особого внимания требуют ситуации, когда беременность наступает у женщин с эрозией.
Обязательно проводится ПЦР-диагностика для исключения инфицирования ВПЧ высокого онкогенного риска.
Как правило, в рутинной практике акушера-гинеколога специально не исследуется такое сочетание, как ВПЧ и беременность.
Анализы на вирус рекомендуются только при обнаружении патологических отклонений.
В то же время существуют исследовательские работы, демонстрирующие влияние вируса на наступление беременности.
Так, было показано, что инфицирование женщин ВПЧ несколько снижает вероятность приживания эмбриона, а у мужчин уменьшает подвижность сперматозоидов.
А поскольку в семейной паре, как правило, инфицированными оказываются оба партнера, то наступление беременности сопряжено с некоторыми трудностями.
В результате при планировании беременности на фоне инфекции, вызванной ВПЧ, планировании процедуры ЭКО следует учитывать и этот фактор.
Как диагностируется ВПЧ у беременных?
В первую очередь диагностика инфекции начинается с клинического осмотра.
Остроконечные кондиломы, как и другие виды образований, легко выявляются по внешнему виду.
При наличии кондилом обязателен осмотр и шейки матки.
В большинстве случаев инфицирование ВПЧ диагностируется на основании ПАП-теста, являющегося первичным скринингом предраковых изменений и рака шейки матки, спровоцированных действием вируса.
Цитологическое исследование по Папаниколау представляет собой вариант микроскопического исследования с применением различных групп красителей.
Существуют характерные признаки изменения клеток, обнаруживаемые в ходе данного исследования, которые свидетельствуют в пользу инфицирования вирусом папилломы.
К таким признакам относятся:
- койлоцитоз – изменение формы и окраски ядра, увеличение количества ядер, появление вакуолей в клетке;
- появление дискерацитов – мелких клеток с окрашенными ядрами и измененной цитоплазмой.
Еще один анализ на ВПЧ при беременности – это типирование папилломавирусов методом полимеразной цепной реакции (ПЦР).

Однако, такое исследование из-за высокой чувствительности часто приводит к гипердиагностике заболеваний, так как в большинстве случаев инфицирование носит кратковременный характер.
Данный метод имеет значение, когда ВПЧ обнаруживается на фоне характерной клинической картины.
В результате мировые медицинские руководства не рекомендуют использовать ПЦР в качестве прогностического анализа женщинам до 30-ти лет.
В старшем же возрасте подобное исследование, особенно в случае определения групповой принадлежности вируса, является более значимым.
При необходимости дополнительно прибегают к инструментальным методам диагностики, таким как кольпоскопия и уретроскопия.
Кольпоскопия и биопсия с гистологическим исследованием проводятся всем женщинам с выявленными в ходе ПАП-теста неоплазиями.

При кольпоскопии также осуществляется тест с уксусной кислотой и раствором Люголя.
Кольпоскопический признак ВПЧ-инфекции – неравномерное окрашивание йодным раствором, побледнение участков после обработки кислотой.
Как проводится лечение ВПЧ инфекции при беременности?
При инфицировании ВПЧ беременность и роды имеют некоторую специфику.
Так, у некоторых женщин с ВПЧ-инфекцией при наступлении беременности могут усиливаться проявления заболевания, такие как изменения клеток шейки матки, остроконечные кондиломы.
Тем не менее, врачи обычно не торопятся с назначением лечения.
Поскольку последнее может спровоцировать преждевременные роды, к тому же, после родов проявления инфекции могут заметно уменьшиться сами по себе.
Поэтому рекомендуется по возможности придерживаться выжидательной тактики и динамического наблюдения за беременной.
Однако случаются ситуации, когда генитальные бородавки заметно разрастаются, увеличивается их количество.
Они сливаются в гигантские образования.
Женщины при этом могут испытывать болезненность при ходьбе, затруднения при дефекации и мочеиспускании.
В родах – травматизацию образований, кровотечение, проблемы с прохождением плода по родовым путям, разрывы влагалищных стенок.
В подобных случаях необходимо удалить кондиломы до родов.
Если же устранение образований не получилось провести вовремя, врач может принять решение о родоразрешении пациентки посредством кесарева сечения.
В рутинной практике эта мера для профилактики инфицирования плода не применяется.
Поскольку нет достоверных данных, подтверждающих, что кесарево сечение препятствует развитию у детей больных матерей респираторного папилломатоза.
Если во время беременности были обнаружены аномальные изменения клеток, то спустя несколько недель после родов следует провести повторное исследование мазка по Папаниколау.
Зачастую после родов и генитальные бородавки, и клеточные изменения сами по себе исчезают.
Соответственно, не требуется и лечение таких состояний.
В иных ситуациях проводят определенные терапевтические процедуры.
У беременных удаление кондилом можно проводить посредством криотерапии, с помощью углекислотного лазера, электрокоагуляции, сургитрона.
При крупных, легкотравмируемых образованиях рекомендуют удалять их хирургическим путем после первого триместра до 36-й недели беременности.
Использование таких препаратов, как подофиллин, 5-фторурацил, а также применение внутриочагового введения интерферона не допускается во время беременности.
Как предотвратить заражение ВПЧ инфекцией?
На сегодняшний день профилактика инфицирования вирусом папилломы проводится посредством введения бивалентной или квадривалентной вакцины.
Бивалентная вакцина активна в отношении вирусов высокой онкогенности 16-го и 18-го типов.
Квадривалентная еще и от вирусов низкой онкогенности 6-го и 11-го типа (основной причины аногенитальных кондилом).
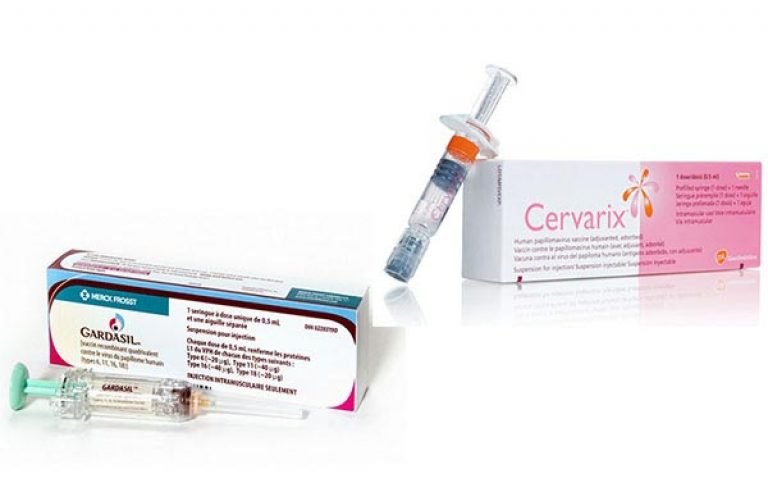
Подобная вакцинация эффективна при ее применении у неинфицированных женщин, то есть до начала последними половой жизни.
Поэтому в некоторых странах она включена в график прививок для девочек до 12-ти лет (в разных странах возраст бесплатной вакцинации отличается).
Прививка может назначаться и женщинам до 26-ти лет при условии наличия у них инфицирования только одним или двумя вирусами.
Вакцинация не исключает необходимости ежегодного скрининга на рак шейки матки, так как она предотвращает только эпизоды заболевания, обусловленные именно ВПЧ.
Вакцинация проводится и неинфицированным мужчинам с целью профилактики рака полового члена.
Что касается использования презерватива при половом контакте, то этот метод немного уменьшает риск инфицирования папилломавирусом, но не исключает его полностью.
Так как возбудитель может находиться в областях, не защищенных материалом контрацептивного средства, и передаваться при контакте кожных покровов.
Для диагностики и лечения ВПЧ при планировании беременности обращайтесь к опытным гинекологам нашего медицинского центра в Москве.
ВПЧ и беременность

Современный мир пестрит информацией о вирусе папилломы человека. Мы напуганы его способностью вызывать рак шейки матки.
А раз он вызывает рак шейки матки, что же он может натворить во время беременности?

Врага надо знать в лицо. Вирус папилломы человека бывает разным, их более 200 типов. И лишь некоторые из них являются онкогенными, то есть могут вызвать неправильные изменения в клетке, которые впоследствии приведут к раку шейки матки. Наиболее онкогенные типы это 16,18,31 и 33 типы.
Вопрос первый: как он передаётся. Тут вопрос деликатный. Основное – это половой путь. Мужчины чаще бывают транзиторными носителями, а болеют женщины. Такова философия жизни. Может быть и другой контактный путь передачи, сама по себе барьерная контрацепция: презерватив при правильном использовании защищает от передачи ВИЧ-инфекции, гепатита В,С, сифилиса; а от ВПЧ увы и ах не всегда.
Вопрос второй: как он лечится. Если вирус встроился в клетку человека, то вылечить его никак невозможно. Возможно, улучшить состояние иммунитета — на это направлены все препараты, которые может выписать доктор, чтобы улучшить иммунитет и перевести вирус в спящее состояние. Если уже есть вирус-ассоциированные последствия на шейке матки, то есть клетки находятся в состоянии изменения под действием вируса (до рака ещё далеко, но первые «звоночки» надо ловить именно тут), то тогда доктор совершенно справедливо может порекомендовать удалить повреждённые ткани (желательно наиболее щадящим методом, например лазерная вапоризация). Удаление поврежденных тканей — это и профилактика онкологических осложнений и лечение очага хронической инфекции, потому что, как правило, под действием вируса присоединяются условно-патогенные бактерии, которые и вызывают хроническое воспаление шейки матки: хронический цервицит, или доктор может сказать кольпит. Следует отметить, что даже если вирус обнаружился, то в течение двух лет он может уйти – элиминироваться самостоятельно, если женщина следит за своим здоровьем, вовремя лечит воспалительные процессы во влагалище и шейке матки. Так что если у вас обнаружен ВПЧ, то паниковать не стоит, но и откладывать визит к доктору тоже. Такую ситуацию доктор должен взять на контроль.

Таким образом, наличие ВПЧ не является противопоказанием для планирования беременности, это не является тератогенным фактором для плода, не является причиной врождённых пороков развития, синдрома Дауна или каких-либо наследственных заболеваний. Женщине надо чётко понять, что взаимосвязи тут нет, и не пугаться за здоровье будущего малыша. Если женщина является лишь носителем ВПЧ, у неё нет атипических клеток в шейке матке, нет воспалительного процесса в шейке матке, то лечение не только не показано, но и совершенно нет показаний для применения иммуномодулирующих препаратов и использования деструктивных методов на шейке матки. Шейка матки ещё пригодится во время беременности, желательно до её доношенного срока (37-40 акушерских недель). Микробиом человека таков, что нас населяет более 10 тысяч различных микроорганизмов. В их числе и вирусы. Стерильности тут нет, и быть не должно. Должна быть гармония в совместном и дружном проживании, хороший иммунитет и позитивный настрой. Итак, при наличии ВПЧ у женщины, планирующей беременность, необходимо проверить: нет ли воспаления, нет ли атипичных клеток. Эти исследования проводит доктор акушер-гинеколог. И если результаты хорошие, то тут зелёный коридор для планирования рождения и во время беременности опасаться осложнений не стоит.
Если при выявленном ВПЧ всё же есть изменения на шейке матки, тогда необходимо пройти лечение. О грамотных подходах и методах лечения ВПЧ при планировании беременности и при самой беременности мы поговорим в следующей части.
Источник https://www.lvrach.ru/2018/05/15436977
Источник https://kvd-moskva.ru/vpch-i-beremennost/
Источник https://fc-ek.ru/info/articles/ginekologiya/urogenitalnye-infektsii/vpch-i-beremennost/